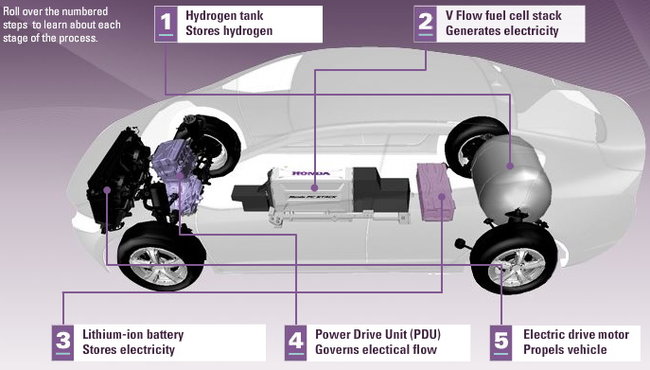
Voiture à hydrogène, une solution écologique?
L’éco-mobilité représente aujourd’hui une question environnementale majeure. Comment accroître le parc de véhicules dits « propres » (voitures électriques ou à hydrogène …)? Quel fonctionnement et quel impact peuvent avoir ces nouveaux moyens de locomotion ?
Depuis quelques temps, les industriels se mobilisent pour lever les obstacles sur le chemin de la voiture à hydrogène.
Une voiture à hydrogène, qu’est ce que c’est ?
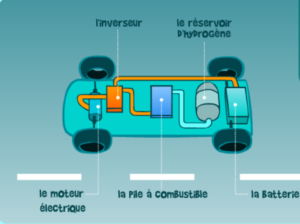
L’élément qui la caractérise est la pile à combustible (ou pile à hydrogène). Ce composant permet la transformation de l’énergie chimique (dihydrogène) en énergie électrique.
Comment est produit ce dihydrogène, stocké dans le réservoir et nécessaire au fonctionnement ?
Le dihydrogène n’existe pas à l’état pur. La méthode de production repose sur le principe de l’électrolyse de l’eau (H2O), qui permet de « fractionner » la molécule à l’aide d’un électrolyseur et de recueillir le dihydrogène convoité (H2).
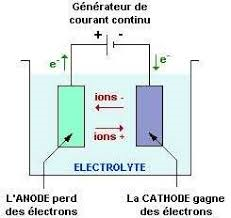
L’expérience se déroule dans une cuve contenant un électrolyte dans laquelle sont plongés 2 électrodes reliés aux bornes d’un générateur. L’ensemble est nommé « cellule d’électrolyse ». L’anode est l’électrode relié au pôle + du générateur, la cathode est reliée au pôle – du générateur.
L’anode est le siège de l’oxydation suivante dans le cas de l’électrolyse de l’eau :
On remarque alors que la molécule d’eau se brise sous l’effet du potentiel électrique auquel elle est soumise, libérant des atomes d’oxygène, des ions H+ ainsi que des électrons. Les atomes d’oxygènes s’accouplent et forment alors du dioxygène. Comme décrit sur le schéma, les ions H+ vont se déplacer de l’anode vers la cathode et les électrons vont circuler dans le circuit externe.
A leur arrivée dans la cathode, les ions H+ vont chercher à se coupler aux électrons et vont alors s’associer à ceux qui circulent dans le circuit externe . On note la réaction de réduction suivante :
Nous obtenons alors du dioxygène sous forme gazeuse. Pour conclure on note alors l’équation red/ox :
Nous remarquons alors que nous recueillons du dihydrogène sous forme gazeuse ainsi que du dioxygène.
Pour information, il nous faut environ 1L d’eau afin de produire 100g de dihydrogène.
Comment stocker le dihydrogène ?
Comme vu dans le premier schéma, la voiture se compose d’un réservoir à hydrogène. Quelle est sa capacité ? Et comment est-il stocké ?
La méthode principalement utilisée dans les voitures actuelles consiste à augmenter la pression du gaz. Ainsi, à 700 bars, l’hydrogène possède une masse volumique de 42 kg/m3. La masse d’hydrogène contenue dans un réservoir spécifié par les constructeurs est typiquement de 4 à 5 Kg pour un véhicule léger (voiture).
Nous somme capables de stocker nos 5Kg d’hydrogène dans un réservoir de 120 litres. En général, 5Kg d’hydrogène constituent une réserve suffisante pour une autonomie de 550 Km en moyenne.
Comment produire l’électricité pour faire fonctionner le moteur ?
Nous avons de l’hydrogène et un réservoir, mais comment produire de l’électricité afin de faire fonctionner le moteur ?
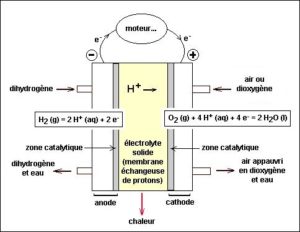
La pile à combustible (ou pile à hydrogène), convertit l’énergie chimique en énergie électrique. Le dihydrogène sous forme gazeuse contenu dans le réservoir est introduit à l’anode, comme décrit dans la précédente partie. Il se déroule un phénomène d’oxydation de forme
H2 (g) = 2 H+ (aq) + 2 e-
La membrane va permettre l’échange de protons et les ions H+ vont alors pouvoir circuler de l’anode vers la cathode. Cependant, les électrons vont devoir emprunter un autre chemin et donc circuler par le circuit externe. Ce débit d’électron crée du courant. Le moteur peut alors fonctionner. La pile alimente directement ce dernier.
Lors de leur arrivée dans la cathode, les ions H+ rencontrent les atomes d’oxygène ainsi que les électrons, qui circulent de l’anode vers la cathode par l’intermédiaire du circuit externe, afin de former de l’eau.
O2 (g) + 4 H+ (aq) + 4 e- = 2 H2O (l)
Il résulte alors de ce phénomène
2 H2 (g) + O2 (g) = 2 H2O (l)
Le seul rejet de cette voiture lors de sa circulation est alors de l’eau !
Atouts, inconvénients et impact écologique
Ainsi, la voiture à hydrogène semble présenter de nombreux atouts : pas d’émission direct de gaz à effet de serre (voir pile à combustible), technologie en constante évolution et avenir prometteur. Mais, il y a aussi quelques inconvénients : prix très élevé (60 000 – 80 000 €), trop peu de station de recharges, et pour le moment … Pas rentable écologiquement !
Jusqu’à aujourd’hui 94% de la fabrication de l’hydrogène reposerait sur les énergies fossiles (chiffres du 04/19). Le bilan est donc pour le moment loin d’être bon (130 grammes de CO2 par km pour la voiture à hydrogène contre 112 pour les voitures à moteur thermique). La méthode par électrolyse fait quant à elle l’objet de nombreuses études, car elle est plus respectueuse de l’environnement, mais elle est aussi 4 fois plus chère (6€ /Kg d’H2) Mais, le développement des nouveaux usages de l’hydrogène-énergie, qui nécessitent un hydrogène plus « pur », ouvre de vastes perspectives à cette technique. Des recherches sont menées pour diminuer le coût de production à travers les énergies vertes …
Sources:
Quelques liens:
https://www.caradisiac.com/quel-avenir-pour-l-hydrogene-113577.htm
https://www.futura-sciences.com/planete/definitions/developpement-durable-voiture-hydrogene-7277/
https://www.futura-sciences.com/sciences/definitions/physique-pile-combustible-3652/
https://fr.m.wikipedia.org/wiki/Émission_de_dioxyde_de_carbone
https://vendre.autobiz.fr/blog/dictionnaire/emissions-co2/
https://www.euro-assurance.com/actualites-assurance/voiture-hydrogene-fonctionnement.html
https://eduscol.education.fr/orbito/pedago/pileh2/pile1.htm
https://www.h2sys.fr/fr/technologies/pile-a-combustible/
https://www.futura-sciences.com/sciences/definitions/physique-electrolyse-339/
https://fr.wikipedia.org/wiki/Électrolyse_de_l%27eau
https://energies.airliquide.com/fr/mediatheque-planete-hydrogene/comment-stocker-lhydrogene
https://fr.wikipedia.org/wiki/Stockage_de_l%27hydrogène
https://www.h2-mobile.fr/dossiers/fonctionnement-voiture-hydrogene-comment-ca-marche/
https://www.usinenouvelle.com/blogs/julien-fosse/l-hydrogene-energie-ideale.N832685
https://www.planete-energies.com/fr/medias/decryptages/comment-fabriquer-l-hydrogene
Un ouvrage:
MPSI Physique-Chimie, Auteur(s) : Finot Thierry, Bonomelli Camille, Choubert Elsa, Daudier Laura, Fayolle Sébastien, Fraticelli Vincen, collection ellipses,